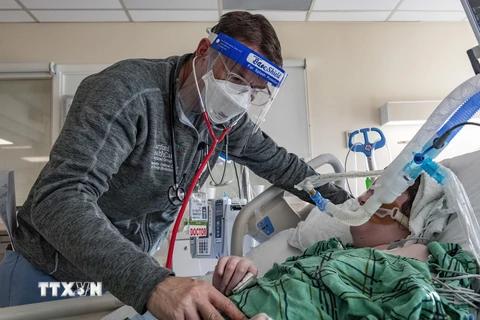
(Nguồn: bloomberg)
(Nguồn: bloomberg) Cơ quan quản lý thực phẩm và dược phẩm Mỹ ngày 16/9 đã phê duyệt ứng dụng liệu pháp gene sinh học do công ty Bluebird phát triển trong điều trị một chứng rối loạn thần kinh hiếm gặp.
Là liệu pháp gene do công ty Bluebird phát triển và thương mại hóa, Skysona được chỉ định sử dụng một lần, để điều trị tình trạng bệnh lý thần kinh do loạn dưỡng não chất trắng thượng thận (CALD) ở bệnh nhân dưới 18 tuổi.
Tuyên bố của Bluebird nêu rõ: "Skysona là liệu pháp đầu tiên được FDA chấp thuận, có tác dụng làm chậm diễn tiến rối loạn chức năng thần kinh ở trẻ em trai."
CALD là một bệnh thoái hóa thần kinh tiến triển và không hồi phục liên quan đến sự phá hủy myelin, lớp vỏ bảo vệ mà các tế bào thần kinh trong não chịu trách nhiệm suy nghĩ và kiểm soát cơ bắp. Các triệu chứng của CALD thường xảy ra ở trẻ em (trung bình 7 tuổi).
Chức năng nhận thức và chức năng thể chất của bệnh nhân suy giảm nhanh chóng và dần dần. Nếu không được điều trị, gần một nửa số bệnh nhân sẽ tử vong trong vòng 5 năm kể từ khi bắt đầu các triệu chứng.
[Tín hiệu tích cực từ ứng dụng AI trong điều trị thoái hóa thần kinh]
Về cơ chế hoạt động, Skysona sử dụng vector lentivirus Lenti-D để truyền trong ống nghiệm, đồng thời chèn bản sao chức năng của gene đột biến ABCD1 vào tế bào gốc tạo máu của chính bệnh nhân.
Việc bổ sung gene ABCD1 chức năng cho phép cơ thể người bệnh có thể sản xuất protein Adrenoleukodystrophy (ALD) có chức năng thực hiện phân hủy sự tích tụ độc hại của các axit béo chuỗi rất dài (VLCFA), chủ yếu ở tuyến thượng thận và chất trắng của não và tủy sống - được xác định là nguyên nhân gây ra CALD.
Từ đó, ngăn chặn sự tiến triển CALD và giúp bảo tồn các chức năng thần kinh, bao gồm bảo tồn chức năng vận động và khả năng giao tiếp.
Trước đây, lựa chọn điều trị duy nhất có sẵn cho bệnh nhân CALD là cấy ghép tế bào gốc từ người hiến tặng phù hợp. Theo Bluebird, liệu pháp Skysona sẽ được triển khai tại các trung tâm điều trị đạt tiêu chuẩn ở Mỹ vào cuối năm nay, song với số lượng hạn chế./.