(Nguồn: channelnewsasia.com)
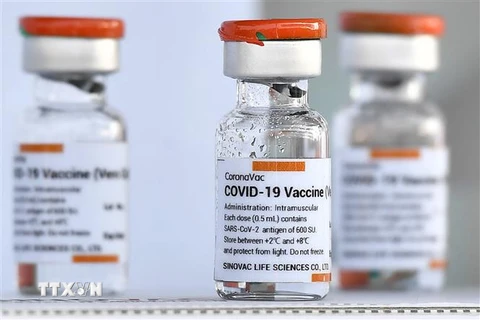
(Nguồn: channelnewsasia.com) Cơ quan Quản lý thực phẩm và dược phẩm (FDA) Mỹ ngày 24/1 đã hạn chế đáng kể việc sử dụng 2 liệu pháp điều trị kháng thể đơn dòng do 2 hãng dược phẩm Eli Lilly và Regeneron bào chế cho các bệnh nhân COVID-19 vì hai liệu pháp này không hiệu quả đối với biến thể Omicron của virus SARS-CoV-2.
Theo phóng viên TTXVN tại Washington, trong thông báo, FDA nêu rõ: "Do dữ liệu cho thấy những liệu pháp điều trị này rất ít khả năng chống lại biến thể Omicron hiện đang lây lan nhanh trên khắp nước Mỹ, nên những liệu pháp này không được phép sử dụng ở bất kỳ bang, vùng lãnh thổ và khu vực pháp lý nào của Mỹ tại thời điểm này."
Ngoài ra, theo FDA, trong tương lai, nếu bệnh nhân ở một số vùng có khả năng bị nhiễm hoặc tiếp xúc với một biến thể mà các liệu pháp điều trị này có hiệu quả, thì việc sử dụng các liệu pháp trên có thể được phép ở những vùng đó. Tuy nhiên, FDA không thu hồi giấy phép sử dụng khẩn cấp đối với các liệu pháp trên.
[Điều trị kháng thể đơn dòng có thể giúp giảm tỷ lệ tử vong do COVID-19]
Liệu pháp điều trị bằng kháng thể hiện nay được khuyến nghị dùng nhiều nhất là Sotrovimab do GlaxoSmithKline và Vir Biotechnology sản xuất.
Chính quyền Mỹ cũng sẽ tiếp tục phân bổ thuốc kháng virus Paxlovid của Pfizer, cũng như thuốc Molnupiravir do Merck bào chế. Tuy nhiên, cả Paxlovid và Sotrovimab đều đang thiếu nguồn cung.
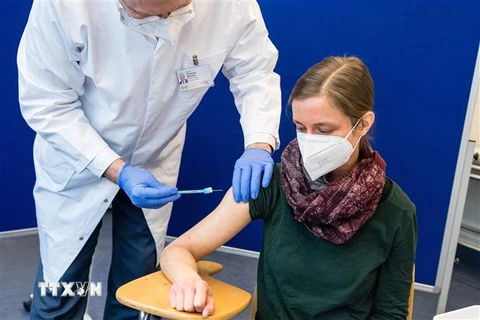
FDA nhấn mạnh rằng các liệu pháp điều trị mặc dù rất quan trọng đối với những bệnh nhân COVID-19 từ nhẹ đến trung bình, những người có nguy cơ cao tiến triển thành bệnh nặng, nhưng không thể thay thế cho việc tiêm chủng.
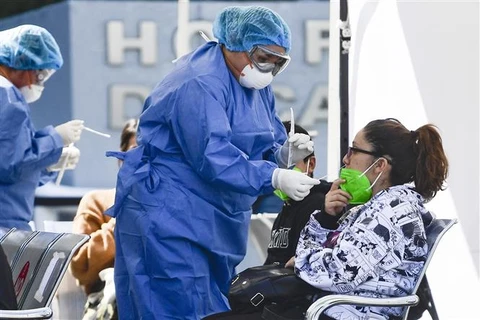
Theo Trung tâm Kiểm soát và Phòng ngừa dịch bệnh (CDC) của Mỹ, biến thể Omicron bắt đầu lan rộng khắp nước Mỹ vào cuối tháng 11/2021 và hiện gây ra 99% các ca mắc mới COVID-19 tại nước này./.